Ewing szarkóma
Az itt megadott összes információ csak általános jellegű, a tumorterápia mindig tapasztalt onkológus kezébe tartozik!
Szinonimák
Csontszarkóma, PNET (primitív neuroektodermális tumor), Askin tumor, Ewing - csontszarkóma
Angol: Ewing-szarkóma
meghatározás
Amiben Ewing szarkóma egy származik Csontvelő kimenő Csontdaganat10 és 30 év között fordulhat elő. Főként a gyermekeket és fiatalokat érinti 15 éves korig. Ewing-szarkóma kevésbé gyakori osteosarcoma.
Az Ewing-szarkóma a régiekben lokalizálódik Hosszú csontok (Combcsont (Combcsont) és Sípcsont (Sípcsont)), valamint a medence vagy a bordákban. Elvileg azonban a törzs és a végső csontváz összes csontja befolyásolhatja, metasztázis különösen a Tüdő lehetséges.
frekvencia
Az Ewing-szarkóma kialakulásának valószínűsége <1: 1 000 000. A tanulmányok kimutatták, hogy minden ott lakó millió emberre évente kb. 0,6 új beteg alakul ki Ewing-szarkóma.
Az osteosarcoma (kb. 11%) és a chondrosarcoma (kb. 6%) összehasonlításában az Ewing-szarkóma a harmadik helyen áll, mint az elsődleges rosszindulatú csonttumorok további képviselője. Míg Ewing-szarkóma elsősorban 10-30 év között fordul elő, a fő megnyilvánulás az élet második évtizedében (15 éves korban) alakulhat ki. Ez elsősorban a növekvő csontvázban nyilvánul meg, ahol a fiúk (56%) valamivel gyakrabban szenvednek Ewing-szarkómában, mint a lányok. Ha összehasonlítjuk a gyermekek és serdülők elsődleges rosszindulatú csontdaganatait, akkor az Ewing-szarkóma a második helyen áll: A gyermekek csontszarkómájában az úgynevezett osteosarcomák aránya körülbelül 60%, az Ewing-sarcomák aránya körülbelül 25%. .
okoz
Amint azt már az összefoglaló összefüggésében kifejtettük és bemutattuk, az oktatás fejlesztéséért felelős ok Ewing szarkóma nem lehet teljesen tisztázni. Megállapítottuk azonban, hogy az Ewing-szarkómák gyakran akkor fordulnak elő, ha családi csontváz rendellenességek vannak, vagy születésük alatt egynél fiatalabb betegek vannak. retinoblasztóma (= serdülőkorban előforduló rosszindulatú retina tumor). A kutatások kimutatták, hogy az Ewing sarcomák úgynevezett családjában lévő tumorsejtek változást mutatnak 22. kromoszóma kiállítás. Úgy gondolják, hogy ez a mutáció az összes beteg 95% -ánál fordul elő.
lokalizáció
Az Ewing-szarkóma leggyakoribb helyei a hosszú csőcsontokban találhatók, különösen a sípcsontban és a combcsontban, vagy a lapos csontokban. Ennek ellenére, mint rosszindulatú csontrák, Ewing-szarkóma az összes csontot érintheti. A nagyobb csontokat a leggyakrabban, a kisebbeket ritkán érinti. Ha a hosszú csöves csontokat érinti, akkor a daganat általában az úgynevezett diaphysis, a tengely területén található.
Előnyben részesített helyek:
- kb. 30% combcsont (combcsont)
- kb. 12% sípcsont (sípcsont)
- kb. 10% gömbcsont (felkarcsont)
- kb. 9% medence
- kb. 8% fibula (fibula).
A korai szakaszban jelentkező súlyos hematogén áttétek miatt (lásd a következő részt) a lágy szövetekben való lokalizáció is elképzelhető.
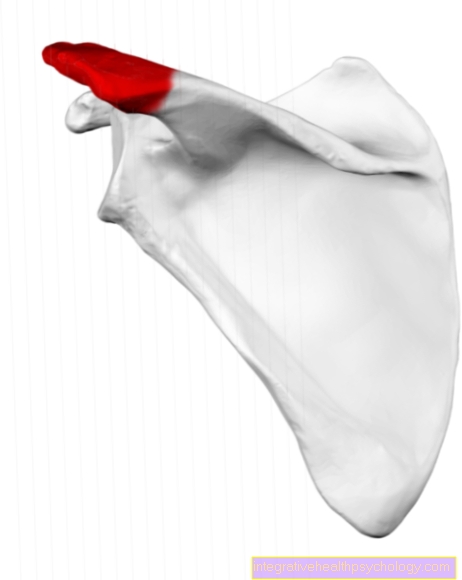
A medence lokalizációja
Az Ewing-szarkóma csak az ötödik esetben lokalizálódik a medencecsontokban, mint elsődleges daganatok (a daganat kiindulási helye). Sokkal gyakrabban azonban az elsődleges daganat egy hosszú csőcsonban található.
Az első tünetek lehetnek duzzanat, fájdalom és túlmelegedés a medence területén.
Lokalizáció a lábban
A láb ritka hely egy primer daganatban. Gyakoribb, hogy a sípcsontból vagy fibulából származó primer daganatok elősegítik a metasztázis kialakulását a lábban.
Ha a láb nem egyértelmű fájdalmas duzzanatot és túlmelegedést mutat, különösen serdülőkorban, akkor a fiatalkori ízületi gyulladás mellett Ewing-szarkómát is ki kell zárni. A legrosszabbat itt nem feltétlenül kell feltételezni. A képalkotás formájában végzett célzott diagnosztika előzetes tisztázást nyújthat a panaszok okairól.
áttétel
Mint fentebb említettük, ez érvényes Ewing szarkóma mint korai hematogén (= a véráramon keresztül) metasztázisos. A metasztázisok tehát a lágy szövetekben is leülepedhetnek. Ezek közül elsősorban a tüdő érinti. A csontvázot azonban a véráramon keresztül áttétek is befolyásolhatják.
Az a tény, hogy Ewing-szarkómát korai áttétes állapotba kell sorolni, azt olyan tanulmányok mutatják, amelyek azt mutatják, hogy a metasztázisok az összes eset körülbelül 25% -ában kimutathatók a diagnózis időpontjában. Mivel az áttétek sajnos nem mindig fedezhetők fel, a sötét arány valószínűleg sokkal magasabb.
diagnózis
Az ewing sarcomák különféle tüneteket okozhatnak. Az alábbiakban kell felsorolni:
- Fájdalom ismeretlen okból
- Duzzanat és általában fájdalom az érintett régió (k) ban
- A nyirokcsomók duzzanata
- helyi gyulladás tünetek (bőrpír, duzzanat, túlmelegedés)
- nem kívánt fogyás
- Funkcionális korlátozások a bénulásig
- Törés baleseti esemény nélkül
- Éjjeli izzadás
- mérsékelt leukocitózis (= a leukociták számának növekedése a vérben)
- csökkent teljesítmény
A daganat elegendő valószínűséggel kizárható, ha a következő kritériumok teljesülnek klinikai, képalkotó és laboratóriumi diagnosztika szerint:
- Nincs bizonyíték a tömegre
vagy
A látható duzzanat, a bevált tömeg vagy a nem egyértelmű panaszok egyértelműen magyarázhatók és dokumentálhatók egy nem daganatos betegséggel.
Alapvető diagnosztika:
Alapvetően képalkotó módszereket használnak az alapvető diagnosztikához. ezek
Röntgen vizsgálat
Röntgenvizsgálat a tumor lokalizációjának területén (legalább 2 szint)
ultrahangvizsgálat
A daganat szonográfia (különösen, ha a differenciáldiagnózisban lágyszöveti daganatot gyanítanak)
További információk beszerzése és a differenciáldiagnosztikai határvonalak lehetővé tétele érdekében laboratóriumi diagnosztikát (laboratóriumi értékek vizsgálata) használnak. A laboratóriumi diagnosztika részeként a következő értékeket határozzuk meg:
- Vérszámlálás
- Vas (mert csökkent a daganatokban)
- Elektrolitok (a hiperkalcémia kizárására)
- ESR (ülepedési sebesség)
- CRP (C-reaktív protein)
- lúgos foszfatáz (aP)
- csontspecifikus (AP)
- Savas foszfatáz (sP)
- Prosztataspecifikus antigén (PSA)
- Húgysav (HRS): növekszik a magas sejtforgalom mellett, pl. hemoblastosisban
- Teljes fehérje: csökkent a fogyasztási folyamatokban
Fehérje elektroforézis - Vizelet állapota: paraproteinek - a mielóma (plazmacitóma) bizonyítéka
- NSE tumor marker = neuron-specifikus enoláz Ewing-szarkómában
Speciális daganatdiagnosztika
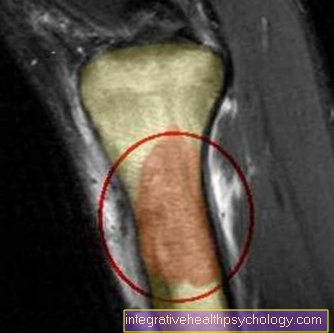
Mágneses rezonancia képalkotás (MRI)
Az alapdiagnosztika összefüggésében említett képalkotó módszerek mellett a mágneses rezonancia tomográfia további lehetőséget jelent, amelyet egyedi esetekben lehet felhasználni.
Az MRI (mágneses rezonancia tomográfia) alkalmazásával a lágy szövetek különösen jól mutathatók ki, ezáltal megmutatható a daganat kiterjedése az érintett csontok szomszédos szerkezeteire (idegek, érek). Ezenkívül az MRI (mágneses rezonancia tomográfia) segítségével megbecsülhető a daganat térfogata, és tisztázható a daganat lokális kiterjedése.
Amint rosszindulatú csonttumor gyanúja merül fel, az egész daganatot hordozó csontot le kell ábrázolni, hogy kizárják a metasztázisokat (rosszindulatú települések).
Számítógépes tomográfia (CT):
(különösen a kemény (kérgi) csontszerkezetek megjelenítésére)
Pozitron emissziós tomográfia (PET)
(Az érték még nem elég érvényes)
További információ a témáról: Pozitron emissziós tomográfia
Digitális kivonás angiográfia (DSA) vagy angiográfia a tumorerek megjelenítéséhez
Csontváz szcintigráfia (3 fázisú szcintigráfia)
szövettani vizsgálat
Mint fentebb már többször említettük, meglehetősen nehéz lehet különbséget tenni például az Ewing-szarkóma és az osteomyelitis között. Amellett, hogy a tünetek hasonlóak, a röntgen önmagában nem mindig ad közvetlen információt. Ha a fent leírt úgynevezett nem invazív diagnosztizálás után továbbra is fennáll a daganat gyanúja, vagy ha bizonytalan a tumortípus és méltóság, a hisztopatológiai vizsgálatot (= szövetvizsgálatot) kell elvégezni.
Nyílt eljárások
Inklinális biopszia
Az úgynevezett incizionális biopszia részeként a daganat részlegesen műtétileg van kitéve. Végül szövetmintát vesznek (ha lehetséges, csontot és lágy szövetet). Az eltávolított tumorszövet közvetlenül megbecsülhető.
Exkluzív biopszia (teljes daganat eltávolítás)
Ezt csak kivételes esetekben veszik figyelembe, például ha gyanú merül fel a kisebb osteochondrómák rosszindulatú daganatainak változására (jóindulatútól rosszindulatúvá).
terápia
A terápiás megközelítés itt általában több szintű. Egyrészről, az úgynevezett terápiás terv általában kemoterápiás kezelést ír elő preoperatív úton (= neoadjuváns kemoterápia). Az Ewing-szarkóma műtéti eltávolítása után a terápiás utánkövetési kezelést sugárterápiával és, ha szükséges, megújított kemoterápiával biztosítják. Itt észrevehető az osteosarcoma különbsége: Az Ewing-szarkómához viszonyítva az osteosarcoma alacsonyabb sugárérzékenységgel rendelkezik.
Terápiás célok:
Az úgynevezett gyógyító (gyógyító) terápiás megközelítést különösen azoknál a betegeknél alkalmazzák, akiknél az Ewing-szarkóma lokalizált és nem mutat áttétet. Időközben az ún. Neoadjuváns kemoterápia a műtéttel és a sugárterápiával kombinálva további lehetőségeket nyit meg. Ha az Ewing-szarkóma a tüdőn kívül áttételt mutat (= generalizált daganatos betegség; extrapulmonalis metasztázisok), akkor a terápiának általában palliatív (életet meghosszabbító) jellege van (lásd alább).
Terápiás módozatok:
helyi:
- preoperatív kemoterápia
- műtéti terápia (széles vagy radikális rezekció az Enneking után)
- sugárkezelés
szisztémás:
daganatellenes kemoterápia
- Kombinált terápia (elsősorban (= "első sor"): doxorubicin, ifosfamide, A metotrexát / Leukovorin, ciszplatin; a második sorban (= "második sor"): etopozid és karboplatin)
(A protokollok rövid időn belül megváltozhatnak)
Gyógyító terápia:
- agresszív több anyagú kemoterápia elő- és posztoperatív módon
- Helyi kezelés csak műtéti daganatos rezekció vagy sugárterhelés formájában
- Kiegészítse a kezelést Pre-besugárzás (például nem működőképes daganatok esetén, nem reagálók) vagy utókezelés útján
- A műtéti terápia kapcsán fontos megemlíteni, hogy nem utolsósorban a műtéti módszerek továbbfejlesztése miatt sok esetben lehetséges a végtagokat megőrző beavatkozás. A gyógyítás lehetősége azonban mindig kiemelt fontosságú, tehát a radikalitásra (= onkológiai minőségre) kell összpontosítani, és nem a funkció esetleges elvesztésére.
- A kemoterápia ezután folytatható (lásd fent). Ezután az úgynevezett konszolidációról beszélünk.
- Tüdőmetasztázisban szenvedő betegek esetén további beavatkozásokra lehet szükség a tüdő területén, például a tüdő részleges eltávolítására.
Paliatív (életet meghosszabbító) kezelés:
Azoknak a betegeknek, akiknek generalizált daganatos betegsége van (= extrapulmonalis metasztázisok), az elsődleges daganatot a törzsön kell elhelyezniük és / vagy az elsődleges daganat működésképtelennek bizonyul. Ilyen esetekben általában csak a palliatív terápia lehetséges. Ilyen esetekben a hangsúly általában az életminőség fenntartására irányul, úgy, hogy a terápia a fájdalom enyhítésére és a funkció fenntartására összpontosítson.
előrejelzés
A visszatérések előfordulása erősen függ a metasztázis mértékétől, a preoperatív kemoterápiára adott választól és a tumor eltávolításának „radikális jellegétől”. Jelenleg úgy gondolják, hogy az ötéves túlélési arány körülbelül 50%. Különösen az operatív fejlesztések tették lehetővé a túlélés valószínűségének javítását az elmúlt 25 évben
A túlélési arány csökken az elsődleges metasztázisokkal. Itt a túlélési arány körülbelül 35%.
A gyógyulás esélyei
A többi rákhoz hasonlóan az Ewing-szarkómából való kilábalás esélyét kezdetben külön-külön tekintik, mivel a statisztikák csak az átlagos gyógyulási és túlélési arányokat mutatják.
A gyógyulás esélye növekszik, ha a daganat műtéttel teljes mértékben eltávolítható. Ezt megelőzően kemoterápiával kell megoldani a daganatot. A daganat sebészeti eltávolítása után további kemoterápiát kell végrehajtani a fennmaradó tumorsejtek elpusztítása érdekében.
Ha a daganatet műtét nélkül nem lehet teljes mértékben eltávolítani, a gyógyulás esélye sokkal rosszabb. Itt kell folytatni a kemoterápiával történő utókezelést.
Azokat a daganatokat, amelyeket nem lehet operálni, feltétlenül ki kell besugárzni.
Általánosságban elmondható, hogy az Ewing-szarkóma gyógyításának esélye rosszabb, ha metasztázisok már vannak a diagnózis időpontjában. Ez azt jelenti, hogy a daganat elterjedt és növekszik a test más részén is.
Túlélési arány
A túlélési arányt általában az orvostudományban adják meg, mint az „ötéves túlélési arány” statisztikai értékét. Ez százalékban jelzi, hogy mekkora a túlélők száma 5 év után egy meghatározott betegcsoportban. A bejelentett Ewing-szarkóma túlélési aránya 40% és 60–70% között van. Ezek a széles területek abból a tényből származnak, hogy a túlélési arány az adott csont régió fertőzésétől függ. Például, ha a karok és / vagy a lábak csontjai érintettek, az ötéves túlélési arány 60–70%. A medencecsontok 40% -át érinti.
Mennyire magas a visszaesés kockázata?
Az ötéves túlélési arány átlagosan 50%. Itt feltételezhető, hogy agresszív és rosszindulatú rák. Az ötéves túlélési arány szerint a diagnosztizált Ewing-szarkómák átlagosan halálához vezetnek.
Ha azonban az Ewing-szarkóma sikeres kezelése után öt év elteltével nem találhatók további leletek, akkor azt mondják, hogy a rák gyógyul.
Utógondozás
ajánlások:
- az 1. és a 2. évben:
Háromhavonta klinikai vizsgálatot kell végezni. Rendszerint egy helyi röntgenvizsgálat, laboratóriumi vizsgálatok, a CT mellkas és teljes test váz-szcintigráfiát végeztünk. A helyi MRI-t általában hathavonta egyszer kell elvégezni. - a 3–5. évben:
Hathavonta klinikai vizsgálatot kell végezni. Rendszerint egy helyi röntgenvizsgálat, laboratóriumi vizsgálatok, a CT mellkas és teljes test váz-szcintigráfiát végeztünk. Helyi MRI-t általában évente egyszer végeznek. - A 6. évetől kezdve az alábbiakat általában évente egyszer kell elvégezni
röntgenvizsgálat laboratóriumi vizsgálattal és a mellkas CT-jével, valamint a teljes test váz-szcintigráfiával és helyi MRI-vel.
összefoglalás
A betegség (Ewing-szarkóma) a nevét James Ewing 1921-es első leírásából kapta. Ezek nagyon rosszindulatú daganatok, amelyek degenerált primitív neuroektodermális sejtekből (= idegsejtek éretlen prekurzor sejtjeiből) származnak. Így az Ewing sarcomák a primitív, rosszindulatú, szilárd daganatokhoz tartoznak.
Mint fentebb már említettük, az Ewing sarcomák elsősorban a hosszú csöves csontok és a medence középső területeit érintik, de elképzelhető a felkar (= humerus) vagy a bordák is, így párhuzamok jelentkeznek az oszteoszarkómával. A kísérő gyulladásos tünetek miatt az összetéveszthető az osteomyelitis-szel.
A nagyon gyorsan előforduló áttétek miatt (a betegek kb. ¼-jén a diagnózis időpontjában már úgynevezett lányos települések mutatkoznak), az Ewing-szarkómák a lágy szövetekben is megtalálhatók, hasonlóan a rabdomioszarkomákhoz. A tüdőket általában a legjobban az áttétek érintik.
Még nem ismertek azok az okok, amelyek felelősek lehetnek az Ewing-szarkóma kialakulásáért. Jelenleg feltételezik, hogy sem a már elvégzett genetikai összetevő (öröklődés), sem a sugárterápia nem felelős a fejlődésért. Megállapítottuk azonban, hogy az Ewing-szarkómák gyakran akkor fordulnak elő, ha családi csontváz rendellenességek vannak, vagy amikor a betegek születésekor retinoblasztómában (= serdülőkorban kialakuló rosszindulatú retina daganatban) szenvednek. A kutatások kimutatták, hogy az úgynevezett Ewing sarcomas család tumorsejtjei változást mutatnak a 22. kromoszóma számán. Feltételezzük, hogy ez a mutáció (genetikai változás) az összes beteg 95% -ánál fordul elő.
Az ewing sarcomák duzzanatot és fájdalmat okozhatnak az érintett régió (k) ban, amelyek funkcionális károsodásokhoz is társulhatnak. A láz és a mérsékelt leukocitózis (= a leukociták számának növekedése a vérben) szintén elképzelhető. A csontritkulással való összetéveszthetőség miatt (például fent) a diagnózis nem mindig könnyű, ezért a képalkotó eljárásokon (röntgenvizsgálat) kívül szükség lehet biopsziára (= szövetminta szövetvizsgálata).
A terápiás megközelítés itt általában több szintű. Egyrészről az úgynevezett terápiás terv általában kemoterápiás kezelést ír elő preoperatív úton (= neoadjuváns kemoterápia). Az Ewing-szarkóma műtéti eltávolítása után a terápiás utánkövetési kezelést sugárterápiával és, ha szükséges, megújított kemoterápiával biztosítják. Itt észrevehető az osteosarcoma különbsége: Az Ewing-szarkómához viszonyítva az osteosarcoma alacsonyabb sugárérzékenységgel rendelkezik.
Az, hogy előfordulnak-e visszatérések (megújult daganatos növekedés), az erősen függ a metasztázis mértékétől, a preoperatív kemoterápiára adott választól és a daganat eltávolításának "radikális jellegétől". Jelenleg úgy gondolják, hogy az ötéves túlélési arány körülbelül 50%. Különösen az operatív fejlesztések tették lehetővé a túlélés valószínűségének javítását az elmúlt 25 évben